Contenuto
- stadi
- Metodo 1 Analizzare la velocità di reazione
- Metodo 2 Traccia un grafico dai dati
- Metodo 3 Risolvi il problema sperimentalmente
È spesso indispensabile sapere come la concentrazione di sostanze chimiche influenza la velocità di una reazione per comprendere i vari processi chimici. "Ordine di reazione" riguarda il modo in cui la concentrazione di uno o più reagenti modifica la velocità di reazione. L'ordine generale di una reazione chimica è la somma degli ordini di reazione di tutti i reagenti presenti. Non sarà sufficiente osservare l'equazione di equilibrio di una reazione per determinarne l'ordine, ma è possibile dedurre questa informazione dalla sua velocità di reazione o dal grafico che la rappresenta.
stadi
Metodo 1 Analizzare la velocità di reazione
-

Analizza l'equazione della velocità. L'equazione della velocità di reazione può aiutarti a determinare l'ordine di reazione. Questa equazione serve a evidenziare l'aumento o la diminuzione di una delle sostanze chimiche in funzione del tempo trascorso. Nessun altro tipo di equazione correlata a questa reazione ti permetterà di identificare il suo ordine di reazione. -

Identificare l'ordine dei reagenti. Ogni reagente nell'equazione della velocità avrà un esponente di 0, 1 o 2 (è estremamente raro incontrare esponenti maggiori di 2). Tutto quello che devi fare è considerare il valore di questo espositore, che ti dirà l'ordine di ciascun reagente.- Se l'esponente è zero, la concentrazione del reagente in questione non influenza la velocità di reazione.
- Se l'esponente è uguale a 1, ciò significa che aumentando la concentrazione del reagente interessato si aumenta linearmente la velocità di reazione (se si raddoppia la sua concentrazione, si raddoppia la velocità di reazione).
- Se l'esponente è 2, la velocità di reazione aumenta esattamente aumentando la concentrazione del reagente (se si raddoppia la sua concentrazione, la velocità viene moltiplicata per 4).
- Il più delle volte, poiché qualsiasi numero elevato a zero sarà sempre 1, i reagenti di ordine zero non sono menzionati nelle equazioni di velocità.
-

Aggiungi l'ordine di tutti i reagenti. L'ordine generale di una reazione chimica è la somma degli ordini di ciascuno dei suoi reagenti. Quindi devi solo sommare gli esponenti di tutti i reagenti per trovare l'ordine della tua reazione chimica. In generale, questo risultato è inferiore o uguale a 2.- Ad esempio, se il tuo reagente numero uno è il primo ordine (ovvero, ha un esponente di 1) e anche il tuo reagente numero due è il primo ordine (ha anche un esponente di 1), quindi la reazione generale sarà di secondo ordine.
Metodo 2 Traccia un grafico dai dati
-

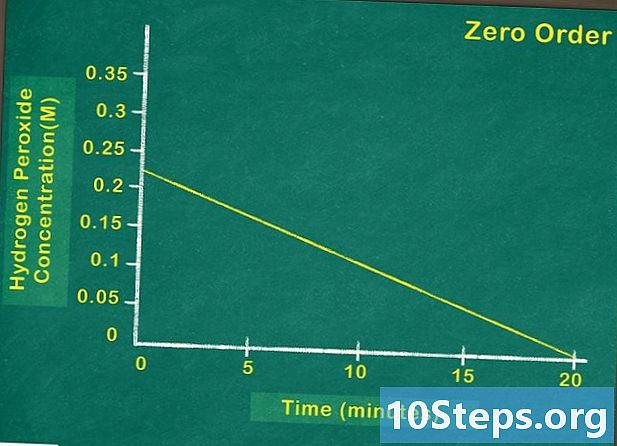
Trova le variabili per rappresentare la reazione con una funzione lineare. Si dice che il grafico che rappresenta la reazione è lineare quando la sua velocità di aumento è costante. In altre parole, significa che la variabile dipendente cambierà tanto nel primo secondo quanto nel secondo, terzo e così via. Visivamente, il grafico a linee apparirà sulla pagina come una linea retta. -

Rappresenta la concentrazione del reagente nel tempo. Puoi vedere sul grafico la quantità di reagente che rimane in qualsiasi momento della reazione. Se la funzione rappresentata nel grafico è lineare, significa che la concentrazione del reagente non ha alcun impatto sulla velocità della reazione. Pertanto, ci si trova di fronte a un reagente di grado zero. -
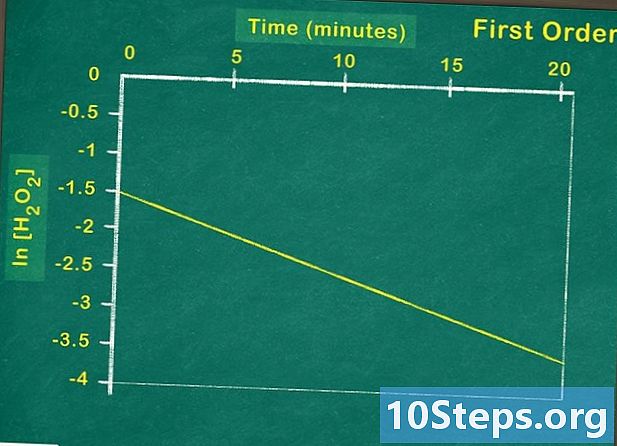
Disegna il logaritmo naturale. Se, rappresentando il logaritmo naturale della concentrazione del reagente in funzione del tempo, si ottiene una funzione lineare, significa che il reagente è del primo ordine. In caso contrario, sarà necessario verificare dal grafico che si tratti di una reazione del secondo ordine. -

Rappresenta l'inverso della concentrazione del reagente rispetto al tempo. Se la funzione corrispondente è una funzione lineare, è perché hai a che fare con una reazione di secondo ordine. Pertanto, la velocità di reazione aumenterà esattamente rispetto all'aumento della concentrazione del reagente. Se la funzione che trovi non è lineare, è perché hai una reazione di ordine zero o del primo ordine. -

Sommare gli ordini di tutti i reagenti. Dopo aver stabilito una funzione lineare per tutti i reagenti, è possibile conoscere l'ordine di ciascuno di essi. È quindi possibile calcolare l'ordine generale. Tutto quello che devi fare è sommare gli ordini dei diversi reagenti per ottenere l'ordine generale della tua reazione.
Metodo 3 Risolvi il problema sperimentalmente
-

Individua un reagente del primo ordine. Scopri qual è l'ordine di una reazione quando la velocità della reazione raddoppia se la concentrazione di uno dei reagenti è raddoppiata. Tenere presente che raddoppiare la concentrazione di un reagente e raddoppiare la velocità di reazione significa che il reagente è di primo ordine. In questo caso, entrambi i reagenti sono del primo ordine. È quindi possibile concludere che la somma di questi due reagenti del primo ordine provoca una reazione chimica del secondo ordine. -

Individua un reagente di ordine zero. Determinare l'ordine di una reazione per la quale non si verifica alcun cambiamento nella velocità di reazione quando si raddoppia la concentrazione di entrambi i reagenti. Se il raddoppio della concentrazione di uno dei reagenti non provoca una variazione della velocità di reazione, significa che il reagente in questione è di ordine zero. In questo caso, i due reagenti sono di ordine zero. Se si mescolano due reagenti di ordine zero, si ottiene una reazione chimica globale di ordine zero. -

Individua un reagente di secondo ordine. Trova quale ordine è una reazione la cui velocità è quadrupla quando uno dei reagenti viene raddoppiato. Il reagente che influenza così la velocità di reazione è di secondo ordine. L'altro reagente non avrà alcuna influenza in questo caso e sarà di ordine zero. La somma degli ordini di questi due reagenti sarà due, il che significa che è globalmente una reazione chimica di secondo ordine.


